🌟 Melhore o seu campo desportivo com um auditoria especializada.
🌟 Melhore o seu campo desportivo com um auditoria especializada.

Partilhar no RRSS
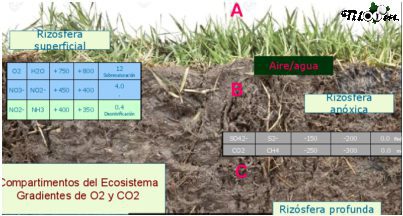
O processos de oxidação-redução exercem um controlo muito importante sobre as concentrações naturais de oxigénio, ferro, metano, etc.... na rizosfera; São também utilizados para determinar os níveis de lixiviação de azoto.
Os processos redox ocorrem através da transferência de electrões de um átomo para outro. A ordem em que ocorrem pode ser prevista a partir da dinâmica do equilíbrio termodinâmico. Estes processos são normalmente muito lentos, a menos que sejam mediados por catálise microbiana. Um exemplo é a redução de sulfatos da matéria orgânica, que seria muito lenta se não fosse a ação microbiana, Desulfovibrio sp, que através de ação enzimática catalisa o processo e a reação pode ocorrer rapidamente em ambientes naturais.
Estes processos redox requerem agentes oxidantes como o oxigénio ou os nitratos. No entanto, a ação de agentes redutores, como a matéria orgânica dissolvida na água dos poros dos nossos perfis verdes, também conduz a estes processos.

Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€
Comprar na Amazon
Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€ Preço: 30€
Comprar na AmazonUm exemplo destes processos pode ocorrer com Fe+2 e Mn +4, como se segue:
2 Fe+2 + MnO2 + 4H+ 2 Fe+3 + Mn+2 + 2H2O
Nesta reação, dois electrões são transferidos do Fe(2) para reduzir o Mn(4) no MnO2. O ião ferroso actua como um redutor e reduz o Mn(4), enquanto o MnO2 pode ser chamado de oxidante e oxida-se a Fe+2. Os electrões são trocados entre os átomos e não existem como "livres" na solução da água dos poros.
A medição de Eh (V), o potencial eletroquímico determina a distribuição de todos os equilíbrios redox, da mesma forma que o pH expressa a distribuição de todos os equilíbrios ácido-base.
A medição é feita através de um elétrodo de platina inerte contra um elétrodo padrão com um potencial conhecido (Grentheet al., 1992 e Christensen et al., 2000).
Assim, podemos observar processos diferentes consoante as medições efectuadas:
Espécies oxidadas Espécies reduzidas mv mv Oxigénio dissolvido (ppm)
O2 H2O +750 +800 12 O2 H2O +750 +800 12 Sobre-saturação
NO3- NO2- +450 +400 4.0
NO2- NH3 +400 +350 0.4 Desnitrificação
Fe+3 Fe+2 +300 +200 +200 0.1 Redução ferrosa
SO4- S2- -150 -200 0,0 Redução de sulfatos
CO2 CH4 -250 -300 0.0 Metanogénese
A utilização de ozono injetado na irrigação mantém o perfil das verduras em condições aeróbias, reforça uma rizosfera bem desenvolvida, neutraliza o consumo de oxigénio pelos biofilmes, e todos os superfícies desportivas apresentam uma maior uniformidade.
O potencial redox da água pode ser conhecido com instrumentos muito acessíveis, tais como:

Agradecemos o seu interesse por nós, por isso deixamos-lhe este formulário para que possa inscrever-se e ter acesso prioritário para o nosso promoções e ofertas exclusivasideal para poupar dinheiro nas suas compras e manter a sua os domínios desportivo e agrícola na vanguarda!
Além disso, mantê-lo-emos informado sobre os NOTÍCIAS MAIS RECENTES em Verdes e Agricultura com as últimas entradas do nosso Greenkeepedia e Agrikipediaincluindo inovações, eventos e entrevistas com especialistas.
Clique para subscrever agora e obter acesso exclusivo!
Uma resposta
Touché! Certos factos. Manter este espírito é um ótimo artigo. Tenho de ler mais blogues como este.
Saudações